Varme vs. temperatur
Indhold
- Indhold: Forskel mellem varme og temperatur
- Sammenligningstabel
- Hvad er Heat?
- Hvad er temperatur?
- Vigtige forskelle
Begrebet varme og temperatur analyseres sammen i matematik, som er noget relateret, men ikke ens. Begge udtryk er almindelige på grund af deres store brug i vores daglige liv. Der findes en fin linje, som afgrænser varme fra temperaturen i den forstand, at varme tænkes på, som en form for energi, men temperaturen er et mål for energi.
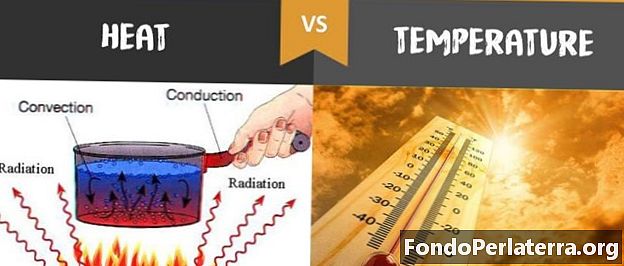
Den største forskel mellem temperatur og varme er lille, men vigtig, varme er molekylbevægelsens generelle energi, mens temperaturen er molekylbevægelsens gennemsnitlige energi. Så lad os se på artiklen, der er givet nedenfor, hvor vi har forenklet de to til dig.
Indhold: Forskel mellem varme og temperatur
- Sammenligningstabel
- Hvad er Heat?
- Hvad er temperatur?
- Vigtige forskelle
- Video forklaring
Sammenligningstabel
| BASIS | VARME | TEMPERATUR |
| Betyder | Varme er mængden af energi i en krop. | Temperatur er målet for varmeintensiteten. |
| Steps | Total kinetisk og potentiel energi indeholdt i molekyler i et objekt. | Den gennemsnitlige kinetiske energi for molekyler i et materiale. |
| Ejendom | Flyder fra varmere genstand til køligere genstand. | Stiger ved opvarmning og falder, når den afkøles. |
| Arbejdsevne | Ja | Ingen |
| Måleenhed | joule | Kelvin |
| Apparat | kalorimeter | Termometer |
| Mærket som | Q | T |
Hvad er Heat?
I fysisk videnskab refererer varme til den energi, der overføres ved hjælp af arbejde eller anden sag. Generelt strømmer varme fra et varmere objekt til et koldere. Denne overførsel resulterer i en netto stigning i entropi. Denne proces kan være direkte, som ved ledning og stråling, i tilfælde af indirekte som i konvektiv cirkulation. Generelt henviser varmeprocessen til overførselsprocessen mellem to systemer, de interesserede systemer og dets omgivelser, der betragtes som et system, ikke som en tilstand eller egenskab for et enkelt system. Mængden af energi, der overføres ved hjælp af varme, udtrykkes i en SI-enhed af joule (J). Varme kan måles ved kalorimetri eller ved hjælp af andre skaleringsteknikker, der er baseret på den første lov om termodynamik. JR Partington - en britisk kemiker - beskriver ledning som: ”Hvis et varmt legeme bringes i kontakt med et koldt legeme, falder temperaturen på det varme krop, og temperaturen i det kolde legeme stiger, og det siges, at en mængde varme passeret fra den varme krop til den kolde krop. ”
Hvad er temperatur?
I fysik refererer temperatur til måling af varme eller kulde i et objekt ved hjælp af et termometer. Forskellige skalaer og enheder bruges til at måle temperatur, ligesom den mest almindelige anvendes er Celsius (betegnet med ° C og også kendt som Celsius), Fahrenheit (betegnet med ° F) og i videnskab med navnet Kelvin (betegnet med K). Temperatur er målet for gennemsnitlig varme eller termisk energi for molekylerne i et stof. For eksempel, når vi siger, at en objekttemperatur er 100 grader, betyder det ikke, at hvert eneste molekyle har den nøjagtige termiske energi. I hvert stof bevæger molekyler sig med en anden række energier og interagerer med hinanden, der ændrer deres energi. Temperatur er lige så vigtig inden for alle videnskabelige områder, såsom biologi, atmosfærisk videnskab, fysik, kemi, geologi, medicin kort sagt i de fleste aspekter af dagligdagen.
Vigtige forskelle
- Varme refererer til mængden af energi i et objekt, mens temperatur betyder måling af varme eller kulde i et objekt.
- Varme betegnes med symbolet på 'Q', mens temperaturen betegnes med symbolet for 'T'.
- Systemets internationale (SI) varmeenhed er joule, mens SI temperaturenhed er kelvin. Mange andre enheder som Celsius og Fahrenheit bruges imidlertid også til temperatur.
- Varme har evnen til at udføre arbejdet, mens temperaturen kun bruges til at måle graden af varme i ethvert stof.
- Varme måles ved hjælp af kalorimetri, mens temperaturen måles ved et termometer.
- Varme er målet for den samlede kinetiske energi for alle molekyler i et stof, mens temperaturen er målet for den gennemsnitlige kinetiske energi for molekyler i et stof.
https://www.youtube.com/watch?v=AUGY9fOmuJY